开发安全高效的新型抗癌手段是目前临床肿瘤治疗亟待解决的关键问题。近年来,利用活性氧打破胞内氧化还原平衡已成为有效杀伤癌细胞的新兴策略,在消除实体肿瘤、重新编程“免疫冷”肿瘤微环境和增强免疫治疗等方面潜力巨大。近期,西安交通大学材料学院钱军民教授课题组基于发现的金属-酰肼配位自组装现象,开发了一系列具有丰富理化性质的金属-酰肼配位纳米药物,研究了其抗癌效果及机制。
1.中空结构的铜/铁双金属-酰肼配位纳米药物用于肿瘤联合治疗(图1)。该研究通过不饱和配位‒刻蚀一体化策略制备了具有中空结构的铜/铁双金属纳米配位物,其中空结构可高效负载化疗药物阿霉素。该纳米药物具有肿瘤微环境触发的催化治疗功能,可特异性放大肿瘤细胞氧化应激并诱导铜/铁超载,实现了铜死亡/铁死亡/凋亡协同杀死肿瘤细胞的目标。该研究提出的不饱和配位‒刻蚀一体化策略为金属纳米药物的设计提供了新思路,有助于促进铜死亡抗肿瘤疗法的发展。该成果以"A Hollow Amorphous Bimetal Organic Framework for Synergistic Cuproptosis/Ferroptosis/Apoptosis Anticancer Therapy via Disrupting Intracellular Redox Homeostasis and Copper/Iron Metabolisms"为题发表于Advanced Functional Materials(IF=19.924)上。论文第一作者为西安交通大学材料学院胥伟军助理教授,通讯作者为西安交通大学材料学院钱军民教授和西安交通大学第一附属医院锁爱莉主任医师。论文链接:https://doi.org/10.1002/adfm.202205013
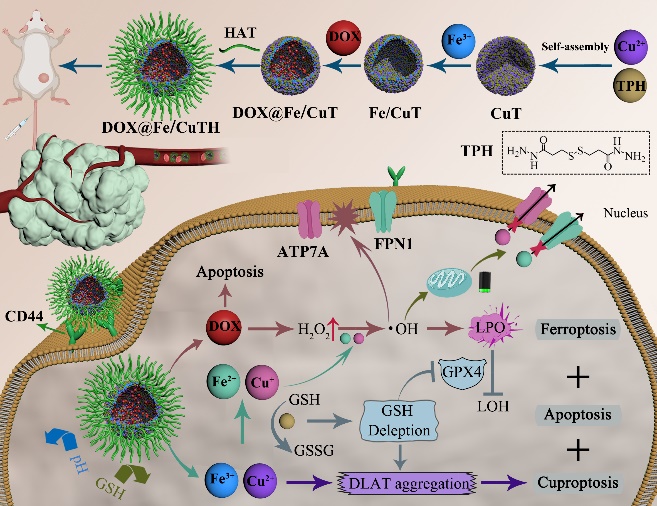
图1 中空铜/铁双金属纳米药物的制备过程及抗肿瘤示意图
2.光热响应型亚铁离子-酰肼配位纳米药物用于增强肿瘤渗透性和铁死亡-凋亡联合治疗。该研究通过一锅自组装法制备了全活性铁-酰肼配位纳米药物。该纳米药物具有良好的光热性能、T2磁共振成像功能和三重刺激响应性降解行为。在近红外光照射下,该纳米药物能渗入肿瘤深部并通过铁死亡-凋亡协同方式有效抑制肿瘤生长。该成果以"Fe(II)-hydrazide coordinated all-active metal organic framework for photothermally enhanced tumor penetration and ferroptosis-apoptosis synergistic therapy"为题发表于Chemical Engineering Journal(IF=16.744)上。论文第一作者为西安交通大学材料学院胥伟军助理教授,通讯作者为西安交通大学材料学院钱军民教授和西安交通大学第一附属医院锁爱莉主任医师,同时该论文得到了西安交通大学生命学院吴道澄教授的大力帮助。论文链接:https://doi.org/10.1016/j.cej.2022.135311
3.核壳结构纳米配位药物用于肿瘤免疫治疗(图2)。利用"grafting from"配位聚合策略,制备了一种具有核壳结构的全活性Cu2O基纳米药物。该纳米药物不但能通过化学动力学/光动力学/化疗三模态联合治疗消除原发性肿瘤,而且能逆转肿瘤“免疫冷”微环境并激活宿主抗肿瘤免疫反应,从而有效抑制远端肿瘤生长、肺转移和肿瘤复发。该成果以"Full-active Cu2O/drug core/shell nanoparticles based on"grafting from"drug coordination polymerization combined with PD-1 blockade for efficient cancer therapy"为题发表于Chemical Engineering Journal(IF=16.744)上。论文第一作者为西安交通大学材料学院博士生侯光晖,通讯作者为西安交通大学材料学院胥伟军助理教授、钱军民教授和西安交通大学第一附属医院锁爱莉主任医师。论文链接:https://doi.org/10.1016/j.cej.2022.135993
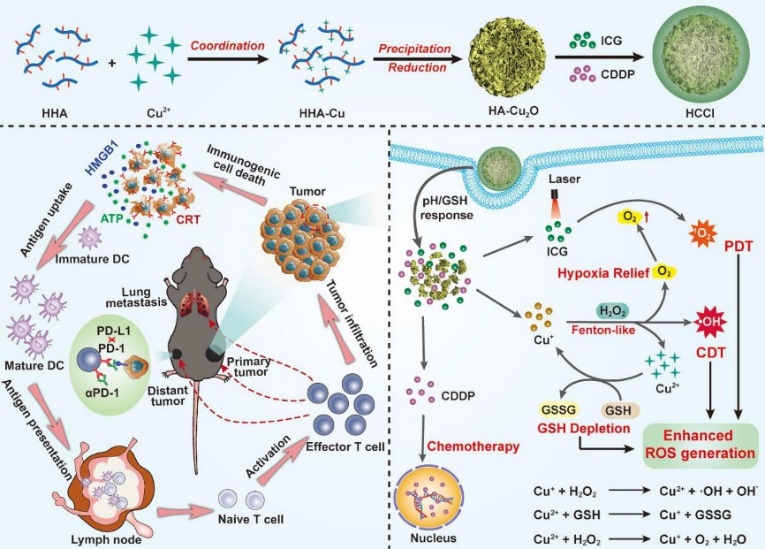
图2 核壳结构Cu2O基纳米药物的制备过程和抗癌机制示意图
4.铜纳米酶/光动力学疗法增强PD-1免疫治疗。通过铜-酰肼配位及原位矿化技术制备了叶片状铜纳米酶,其具有肿瘤微环境响应性降解行为和类芬顿/类谷胱甘肽氧化酶/类过氧化氢酶三重酶活性。该纳米酶能通过生成大量活性氧以消除原发性肿瘤并诱导肿瘤细胞免疫原性死亡,从而有效抑制远端肿瘤生长和肿瘤肺转移。该成果以"Copper coordinated nanozyme-assisted photodynamic therapy for potentiating PD-1 blockade through amplifying oxidative stress"为题发表于Chemical Engineering Journal(IF=16.744)上。论文第一作者为西安交通大学材料学院博士生侯光晖,通讯作者为西安交通大学材料学院钱军民教授和西安交通大学第一附属医院锁爱莉主任医师。论文链接:https://doi.org/10.1016/j.cej.2022.134778
5.酰肼化透明质酸/顺铂/吲哚菁绿配位纳米前药制备及其用于肝癌光动力/化疗联合治疗。该研究通过顺铂-酰肼和顺铂-吲哚菁绿双重配位反应制备了顺铂/吲哚菁绿纳米复合前药,首次观察到顺铂可以诱导吲哚菁绿的J-聚集体由置顶式堆叠转变为头尾式堆叠,其吸收峰由720-780 nm红移至895 nm。该纳米前药具有谷胱甘肽/近红外光双重响应性药物释放行为,能被肝癌细胞有效摄取,并通过光动力/化疗协同的方式杀死肿瘤细胞,抑制肿瘤生长。该成果以"Hydrazided hyaluronan/cisplatin/indocyanine green coordination nanoprodrug for photodynamic chemotherapy in liver cancer"为题发表于Carbohydrate Polymers(IF=10.723)上。论文第一作者为西安交通大学材料学院博士生侯光晖,通讯作者为西安交通大学材料学院钱军民教授和西安交通大学第一附属医院锁爱莉主任医师。论文链接:https://doi.org/10.1016/j.carbpol.2021.118810
6.该课题组还利用上述金属-酰肼配位技术构建了一系列多功能透明质酸水凝胶(图3A)。以铜-酰肼配位透明质酸水凝胶为代表,系统研究了其在皮肤伤口愈合中的作用。该水凝胶呈现自愈合性、可注射性、形状自适性、导电性及多重刺激响应性等功能,具有广谱抗菌活性和促伤口愈合能力,可显著加速感染伤口愈合。该研究为多功能皮肤伤口敷料制备开辟了一条新途径,在生物医学、可穿戴设备和软机器人等前沿领域显示出巨大潜力。该成果以"Copper-Hydrazide Coordinated Multifunctional Hyaluronan Hydrogels for Infected Wound Healing"为题发表于ACS Applied Materials & Interfaces(IF=10.383)上。论文链接:https://doi.org/10.1021/acsami.2c01254

图3(A)酰肼化透明质酸和不同金属离子配位形成的凝胶图片;铜-酰肼凝胶的(B)自愈合性、(C)可注射性和(D)适形性。
上述成果均以西安交通大学金属材料强度国家重点实验室为第一通讯单位。上述工作得到了国家自然科学基金、陕西省重点研发计划、陕西省自然科学基金、中央高校基本科研业务费、中国博士后科学基金等项目的资助。